Metabolism
Metabolism  Cellens ämnesomsättning
Cellens ämnesomsättning  Anabolism
Anabolism  Proteinsyntesen
Proteinsyntesen  Från polypeptidkedja till protein
Från polypeptidkedja till protein
Från polypeptidkedja till protein
I något skede under eller efter translationen vecklas polypeptidkedjan ihop till sin slutgiltiga tredimensionella form. I det cytoplasmatiska nätverket finns olika proteiner, som assisterar vid veckningen. Den rätta konfigurationen är den energetiskt mest fördelaktiga. Den innehåller den största möjliga mängden svaga bindningar (väte-, jon-, van der Waals- och hydrofoba växelverkningar), som stabiliserar polypeptidkedjorna i deras vattenmiljö. Även de s.k. multimera proteinernas sidokedjor binder till varandra på rER membranerna. På så sätt får de sin tertiära struktur. Proteiner, som har vecklats på fel sätt samt ensamma underenheter, förstörs av proteasomerna i cytoplasman.
Fastän alla polypeptidkedjor börjar med aminosyran metionin (M) (eller med N-formylmetionin i bakterier) så spjälks de flesta proteiner av på ett sådant sätt att det i N-terminalen finns en annan aminosyra än M. Även de C-terminala aminosyrorna avlägsnas ofta. Hälften av alla eukaryota proteiner får en acetylgrupp adderad till sin N-terminala aminosyra. I polypeptidkedjans N-terminal finns ofta en signalsekvens bestående av 15-20 aminosyror. Denna signalsekvens leder proteinet till dess rätta plats i cellen. Signalsekvensen avlägsnas av peptidaser innan proteinet får sin riktiga funktion. Vissa proteiner måste undergå proteolytiska behandlingar innan de får sin slutgiltiga funktion. Detta gäller många av våra matsmältningsenzymer.
Det är möjligt att modifiera enstaka aminosyror efter translationen. 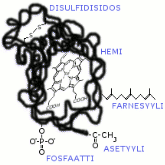
Med hjälp av fosforylering kan man reglera vissa enzymers aktivitet. Då proteiner fosforyleras adderas en fosfatgrupp
från ATP till serinets, treoninets eller tyrosinets hydroxylgrupp. Detta ger dem en stark negativ laddning. I rER-cisternerna kan stabiliserande disulfidbindningar (-S-S-) mellan två cysteiner bildas. På så sätt blir cysteinerna kovalent bundna till varandra.
Översätt bild: DISULFIDBINDNING; HEM; FARNESYL; ACTYL; FOSFAT
För att fungera som de skall behöver många proteiner kovalent bundna prostetiska grupper, såsom hem-gruppen i cytokrom c. Kolhydratkedjorna i glykoproteinerna binds med kovalenta bindningar till polypeptidkedjan med hjälp av vissa aminosyror (asparagin, serin eller treonin). I vissa proteiner binds hydrofoba isoprenylgrupper (såsom farnesyl) till aminosyran cystein. Detta leder till att proteinerna har lättare att fästa vid lipidmembraner.