Polypeptidiketjusta proteiiniksi
Jossain vaiheessa translaation aikana tai sen jälkeen polypeptidiketju laskostuu oikeaan kolmiulotteiseen muotoonsa. Solulimakalvoston ontelossa on erilaisia proteiineja, jotka auttavat polypeptidejä laskostumaan. Oikein laskostunut konformaatio on energeettisesti edullisin, toisin sanoen siinä on suurin mahdollinen määrä heikkoja vuorovaikutuksia (vety- ja ionisidoksia ja van der Waalsin ja hydrofobisia vuorovaikutuksia), jotka stabiloivat vedessä olevaa polypeptidiketjua. Myös multimeeristen proteiinien alayksiköt sitoutuvat toisiinsa rER:llä (tertiäärirakenne). Väärin laskostuneet proteiinit ja yksinäiset alayksiköt hajotetaan soluliman proteasomeissa.
Vaikka kaikki polypeptidiketjut alkavat alun perin metioniinilla (tai N-formyylimetioniinilla bakteereissa), translaation jälkeen useita proteiineja katkaistaan niin, että N-terminaalisessa päässä onkin jokin muu aminohappo. Myös C-terminaalisia aminohappoja poistetaan usein. Noin puoleen eukaryoottien proteiineista myös lisätään N-terminaaliseen aminohappoon asetyyliryhmä. Polypeptidiketjun N-terminaalisessa päässä on usein 15 - 30 aminohapon signaalisekvenssi, jonka perusteella proteiini kuljetetaan oikeaan kohteeseensa solussa. Signaalisekvenssit poistetaan peptidaaseilla ennen proteiinin varsinaista toimintaa. Joistakin proteiineista tulee aktiivisia vasta proteolyyttisen käsittelyn jälkeen (esimerkiksi monet ruoansulatuksen entsyymit).
 Yksittäisiä aminohappoja voidaan muokata translaation jälkeen. Fosforylaatiolla voidaan esimerkiksi säädellä joidenkin entsyymien aktiivisuutta. Proteiineja fosforyloitaessa seriini-, treoniini- tai tyrosiinitähteen hydroksyyliryhmään liitetään ATP:ltä fosfaattiryhmä, joka tuo mukanaan voimakkaan negatiivisen varauksen. Kysteiinien välille voi puolestaan rER:n ontelossa syntyä proteiinin rakennetta stabiloivia disulfidisidoksia (-S-S-), joissa kaksi kysteiiniä on kovalenttisesti sitoutunut toisiinsa.
Yksittäisiä aminohappoja voidaan muokata translaation jälkeen. Fosforylaatiolla voidaan esimerkiksi säädellä joidenkin entsyymien aktiivisuutta. Proteiineja fosforyloitaessa seriini-, treoniini- tai tyrosiinitähteen hydroksyyliryhmään liitetään ATP:ltä fosfaattiryhmä, joka tuo mukanaan voimakkaan negatiivisen varauksen. Kysteiinien välille voi puolestaan rER:n ontelossa syntyä proteiinin rakennetta stabiloivia disulfidisidoksia (-S-S-), joissa kaksi kysteiiniä on kovalenttisesti sitoutunut toisiinsa.
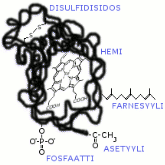
Monet proteiinit tarvitsevat toimiakseen kovalenttisesti kiinnitettyjä prosteettisia ryhmiä, kuten sytokromi c:n hemi-ryhmä. Glykoproteiinien hiilihydraattiketjut kiinnitetään polypeptidiketjuun kovalenttisesti tiettyjen aminohappojen (asparagiini, seriini tai treoniini) välityksellä. Joidenkin proteiinien kysteiinitähteisiin kiinnitetään hydrofobisia isoprenyyliryhmiä (kuten farnesyyli), jotka voivat mm. auttaa proteiineja kiinnittymään lipidikalvolle.