Translokaatio
Translokaatiot ovat tyypillisimpiä rakenteellisia kromosomipoikkeavuuksia. Translokaation seuraksena perintöainesta siirtyy tai vaihtuu kahden, joskus kolmen, kromosomin kesken. Translokaatio vaikuttaa geenitoimintaan jos se katkaisee geenin tai siirtää geenin väärän säätelyalueen alaisuuteen. Kasvutekijägeenin siirtyminen translokaation seurauksena aktiivisen säätelyalueen yhteyteen voi johtaa syövän syntyyn.
Ihmisen yleisin translokaatio on kromosomien 13 ja 14 välinen translokaatio. Translokaatio kromosomista 8 kromosomeihin 14, 2 ja 22 on myös tyypillistä. Burkittin lymfoomaan liittyvässä translokaatiossa osa kromosomista 8 siirtyy kromosomiin 14. Kromosomista 8 siirretty onkogeeni c-myc aktivoituu vasta-ainegeenien läheisyydessä. Toinen syöpiin liittyvä tunnettu kromosomimuutos on translokaatio kromosomista 22 kromosomiiin 9. Tälle on annettu ensimmäisen raportoidun ilmentymisen johdosta nimi Philadelphia-kromosomi. Muutoksen seurauksena c-abl onkogeeni aktivoituu aiheuttaen suurentuneen riskin sairastua krooniseen myeloiseen leukemiaan.
Jos translokaation yhteydessä perintöaines ei lisäänny eikä vähene sanotaan translokaation olevan balansoitunut. Balansoituneen translokaationkin seurauksena voi syntyä esimerkiksi osittaista trisomiaa seuraavassa sukupolvessa. Ajatellaan tilannetta, jossa toisella vanhemmista on translokaation seurauksena yhden normaalin lisäksi toinen kromosomi, joka sisältää ylimääräistä perimäainesta. Epänormaalin kromosomin siirtyessä hedelmöittymisessä eteenpäin seurauksena on aiemmin translokoituneen kromosomin osalta trisomia.
Philadelphia kromosomi
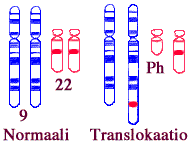 Translokaatio kromosomista 22 kromosomiin 9 saa aikaan ns. Philadelphia kromosomin. Tämä muutos on löydettävissä tietyistä syöpäsoluista (krooninen myelogeeninen leukemia).
Translokaatio kromosomista 22 kromosomiin 9 saa aikaan ns. Philadelphia kromosomin. Tämä muutos on löydettävissä tietyistä syöpäsoluista (krooninen myelogeeninen leukemia).
abl-esisyöpägeeni on solujen viestintään liittyvä tyrosiinikinaasi, joka fosforyloi solussa tiettyjä kohdevalkuaisaineita. Translokaation johdosta abl-esisyöpägeeni ja bcr-geeni yhdistyvät siten, että lopputuotteena on yhdistelmä-valkuaisaine. Normaalisti solun fosforylaatiotapahtumat ovat säädeltyjä, eli ne vaativat sopivan ärsykkeen aktivoituakseen. bcr-abl yhdistelmäproteiini on kuitenkin jatkuvasti aktiivinen, mikä viime kädessä saa aikaan mutaation saaneen kohdesolun transformoitumisen syöpäsoluksi.
Tämän entsyymitoiminnan spesifinen estäjä imatinibi (aiemmin STI 571) on esimerkki modernin syöpätutkimuksen saavutuksista solunsalpaaja-hoitojen kehittämiseksi. Vaikutus perustuu imanitibin kykyyn kilpailla ATP:n sitoutumisesta teittyihin tyrosiinikinaaseihin.
Lääkkeellä on saatu erittäin lupaavia hoitotuloksia kroonisen myelooisen leukemian ja Philadelphia-kromosomin sisältävän akuutin lymfoblastileukemian hoidossa erittäin lievin sivuvaikutuksin. Myös mahasuolikanavan sarkoomassa (GIST), johon liittyy c-kit geenin tyrosiinikinaasin aktivoituminen, imatinibilla on saavutettu hyvä hoitovaste valtaosalla potilaista.