Proteinernas struktur
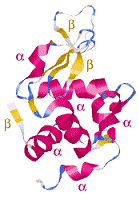
Proteinernas struktur kan studeras på fyra olika nivåer.
Aminosyrornas ordningsföljd i polypeptidkedjan, dvs. aminosyrasekvensen, är den s.k. primärstrukturen.
Primärstrukturen säger mycket lite om proteinernas tredimensionella struktur och funktion.
I proteiner finns tre olika sekundärstrukturer:
1. α-helix
2. β-konformation
3. random-coil
Det enklaste arrangemanget som en polypeptidkedja kan anta är α-helixstrukturen.
I en α-helix är polypeptidkedjan snurrad runt en längdaxel med R-grupperna, som sticker ut från kedjan. Den vanligaste α-helixstrukturen är högervridande och har 3,6 aminosyror per varv. α-helixstrukturen hålls ihop av vätebindningar och är den enda möjliga spiralfomen för en polypeptidkedja. Fibrösa och globulära proteiner består vanligen av α-helixstrukturer.
β-konformationen, som också är en vanlig struktur i proteiner, består av flera närbelägna polypeptidkedjor i ett zig-zagmönster. De hålls ihop av vätebindningar.
Det finns två typer av β-konformationer:
1. parallella, som består av polypeptidkedjor, som löper i samma riktning.
2. antiparallella, som består av polypeptidkedjorna, som löper åt motsatta håll.
Random coil ("β-turn") är den tredje typen av sekundärstruktur. I denna struktur vänder peptidkejdan 180° och formas av fyra aminosyror, vilka är sammanhållna av vätebindningar mellan den första och den fjärde aminosyran. β-turn finns ofta nära ytan av ett protein eller i vändpunkten av en β-struktur.
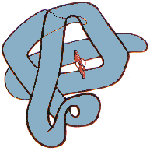
Proteinets tredimensionella struktur bildar tertiärstrukturen. Ifall två eller flere polypeptider bildar en stor komplex molekyl talar man om en kvartärstruktur. Hemoglobin består av två α-kedjor och två β-kedjor. Bilden till vänster visar β-kedjans struktur i hemoglobin.