Cellmembranet
Cellmembranet  Cellmembranets byggnad
Cellmembranets byggnad  Cellmembranets byggnad
Cellmembranets byggnad  Olika typer av proteiner
Olika typer av proteiner  Transmembrana proteiner
Transmembrana proteiner
Transmembrana proteiner
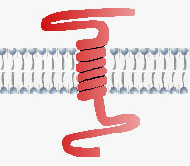
Transmembrana proteiner (kallas även integrala proteiner = IP) har fått sitt namn på grund av att de går igenom det dubbla lipidskiktet en eller flera gånger. Största delen av membranproteinerna hör till denna grupp.
Bilden till höger visar den allmänna strukturen hos ett transmembranprotein. Transmembrana proteiner har både vattenavstötande (hydrofoba) och vattenlösliga (hydrofila) delar. De hydrofoba partierna är fettlösliga och de ligger inne i själva membranet medan de vattenlösliga delarna sträcker sig bort från membranet. Bilden visar glykoforin A i röda blodkroppar. Glykoforin A består av 131 aminosyror. Glykoforin A har många sockergrupper bundna på utsidan av cellen.
Alla hittills kända bärarproteiner och jonkanaler går igenom cellmembranet flera gånger. Ett exempel på detta är band 3 proteinet, som förekommer i röda blodkroppar. Band 3 är ett jonbytesprotein för anjoner och går igenom cellmembranet 12-14 gånger. De transmem- brana proteinerna har vanligtvis en hydrofob a-helix-struktur. Dessutom förekommer b-konformationer i de membranspännande delarna.
Amfipatiska a-helix-strukturer (ena delen = hydrofob; andra delen = hydrofil) kan också bilda transmembrana proteiner (3.0-3.8 nm). För att kunna gå igenom det dubbla lipidskiktet måste a-helixen består av 20-25 aminosyror. b-konformationer (med minst 20 kedjor) kan bilda tunnlika strukturer, som passerar membranet.
På utsidan av cellen har transmembrana proteiner vanligen sockerkedjor fästade vid sig. Största delen av cellernas receptorer är membranbundna. En receptor, som sitter i cellmem-branet, går igenom detta och når insidan. Membranreceptorn förmedlar signalen till cellens insida där den fångas upp av andra proteiner. Ofta sker denna kedjereaktion med hjälp av en serie fosfoyleringar.